白金による酸素の還元反応についてMOPAC2012 PM7法を用いて詳細に調べてみました。
これは家庭用燃料電池や自動車に搭載される燃料電池の空気極で起きている反応で
表面波基底を用いた第一原理計算の例が報告されていますが半経験的分子軌道法であるMOPACでどこまで再現できるでしょうか。
前の記事で酸素分子がプラチナ表面に吸着することを述べましたが、
今回はそこにプロトンが近づくときにどのようになるかを述べます。
[PR] この広告は3ヶ月以上更新がないため表示されています。
ホームページを更新後24時間以内に表示されなくなります。
燃料電池の空気極 -吸着酸素とプロトンとの反応-
ホーム 「量子化学計算で探るミクロの世界」
白金による酸素の還元反応についてMOPAC2012
PM7法を用いて詳細に調べてみました。
これは家庭用燃料電池や自動車に搭載される燃料電池の空気極で起きている反応で
表面波基底を用いた第一原理計算の例が報告されていますが半経験的分子軌道法であるMOPACでどこまで再現できるでしょうか。
前の記事で酸素分子がプラチナ表面に吸着することを述べましたが、
今回はそこにプロトンが近づくときにどのようになるかを述べます。
![]()
次の四つの図はプロトンが水分子と結合したヒドロニウムイオンが吸着酸素に近づく時の変化の様子を示したものです。
図中の数値は各原子の電荷を示しており、吸着酸素の右側の酸素原子のマイナス電荷の値が次第に大きくなり、またヒドロニウムイオンの一水素原子がその酸素原子のほうへ向いて正電荷を大きくしながら近づいて行きます。そしてその水素原子はヒドロニウムイオンから離れて吸着酸素と結合し、水分子が生成しました。また図の下に示した括弧内の数値はそれぞれの状態の生成熱であり、次第に値が小さくなっていることからこの反応が自発的に起こることがわかります。
    3.5Å(1233kcal/m) 3.1Å(1206kcal/m) 3.0Å(1205kcal/m) 2.9Å(1174kcal/m) 以上の計算はすべて電荷+1で行っています。ここで水素原子が酸素と結合した時点でこの系に電子が一個流入すると仮定して電荷0で計算すると下図のようになります。  2.9Å電荷0(945kcal/m) 酸素分子は解離し、OH結合ができています。そして生成熱は大きく下がっており電子が流入するという仮定が正しいことを示しています。電子が流入するとなぜ酸素分子が解離するのでしょうか。その理由を探ってみました。 下図は解離する前の分子軌道の一つで酸素原子間の反結合性軌道です。この軌道は酸素原子のPy軌道でできていて、しかも空気道で電子は入っていません。
それに対して解離後の分子軌道のうち酸素原子のPy軌道を含む軌道はすべて被占軌道で電子が入っており、それが酸素分子を解離させていると思われます。 前の記事にあるように吸着酸素は解離するのに単独ではエネルギー障壁がありましたが、ヒドロニウムイオンの存在する酸性の雰囲気ではずっと解離しやすいことを示しています。 燃料電池の空気極では解離した酸素原子に水素原子が二個結合して水分子ができて反応が完結します。この過程を再現するためOH結合の部分にヒドロニウムイオンを近づけてみました。下図図中の数値は酸素-プラチナ間の原子間距離と結合次数で、2.7Åで水分子ができており酸素原子とプラチナ間の結合はほとんど切れています。ここに電子が一つ流入すると仮定して電荷0で再計算すると結合次数はさらに小さくなり、水分子はプラチナ表面から離れることができます。  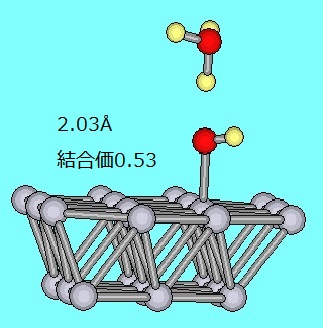   3.5Å(1152kcal/m) 2.8Å(1145kcal/m) 2.7Å(1126kcal/m) 2.7Å電荷0(927kcal/m) 以上のように燃料電池の空気極においては、白金表面に吸着した酸素分子がヒドロニウムイオンの存在する酸性の雰囲気で解離し、水素原子二つと結合して水分子が生成し、その際二つの電子が関係することが示されました。 |